 当前位置:首页 > 研究领域 > 消化系统
当前位置:首页 > 研究领域 > 消化系统
糖尿病(diabetes)是一种以葡萄糖和脂肪代谢紊乱、血浆葡萄糖水平升高为主要临床特点的代谢性疾病,长期的高血糖,导致各种组织,特别是眼、肾、心脏、血管、神经的慢性损害、功能障碍。糖尿病主要分为四类:1型糖尿病、2型糖尿病、妊娠期糖尿病和特殊类型糖尿病,以2型糖尿病(type 2 diabetes, T2D)最为常见。1型或2型糖尿病均存在明显的遗传异质性。1型糖尿病有多个DNA位点参与发病,其中以HLA抗原基因中DQ位点多态性关系最为密切。2型糖尿病已发现多种明确的基因突变,如胰岛素基因、胰岛素受体基因、葡萄糖激酶基因、线粒体基因等。
2020年,南京医科大学韩晓教授研究团队在《Diabetes 》上发表的“HRD1 an important player in pancreatic β-cell failure and therapeutic target for type 2 diabetic mice”论文研究表明胰岛β细胞中HRD1的特异性过表达引发胰岛素分泌受损,最终导致严重高血糖。该研究成果发现HRD1可作为2型糖尿病的治疗靶点,使人类在治疗T2D方面又取得新进展!

HRD1 (HMG-CoA reductase degradation 1),是内质网应激相关E3泛素连接酶的代表,通过靶向并有效降解错误折叠的胰岛素原维持胰岛β细胞的功能,HRD1的缺失会导致胰岛素分泌(GSIS)受损。研究报道HRD1在 Akita糖尿病小鼠胰岛中表达上调。NCBI GEO数据库的基因组数据显示,T2D患者胰岛细胞HRD1 mRNA水平升高。然而,HRD1在胰岛β细胞中的特异性病理作用仍不明确。
通过Western blot、qRT-PCR和免疫荧光染色方法,作者发现:① db/db和HFD饲料喂养的糖尿病小鼠胰岛中HRD1显著上调;② T2D患者分离的胰岛也得到了类似的结果;③db/db和HFD饲喂的小鼠胰腺β细胞内质网HRD1显著升高,伴随胰岛素水平的显著降低;④ 长期暴露于高糖环境的人及小鼠胰岛细胞HRD1表达较正常组明显上调;⑤ 在慢性高糖处理的人胰岛初级β细胞中HRD1表达增强。综上所述,糖尿病人及小鼠胰腺β细胞HRD1表达水平升高,可能与β细胞的衰竭和糖尿病的发生有关。

作者将AAV-MIP-shHRD1-GFP(维真生物提供)注射入雄性C57BL / 6J小鼠胰腺导管,特异性敲低小鼠β细胞中的HRD1。免疫荧光观察显示AAV病毒在体内有效传递。
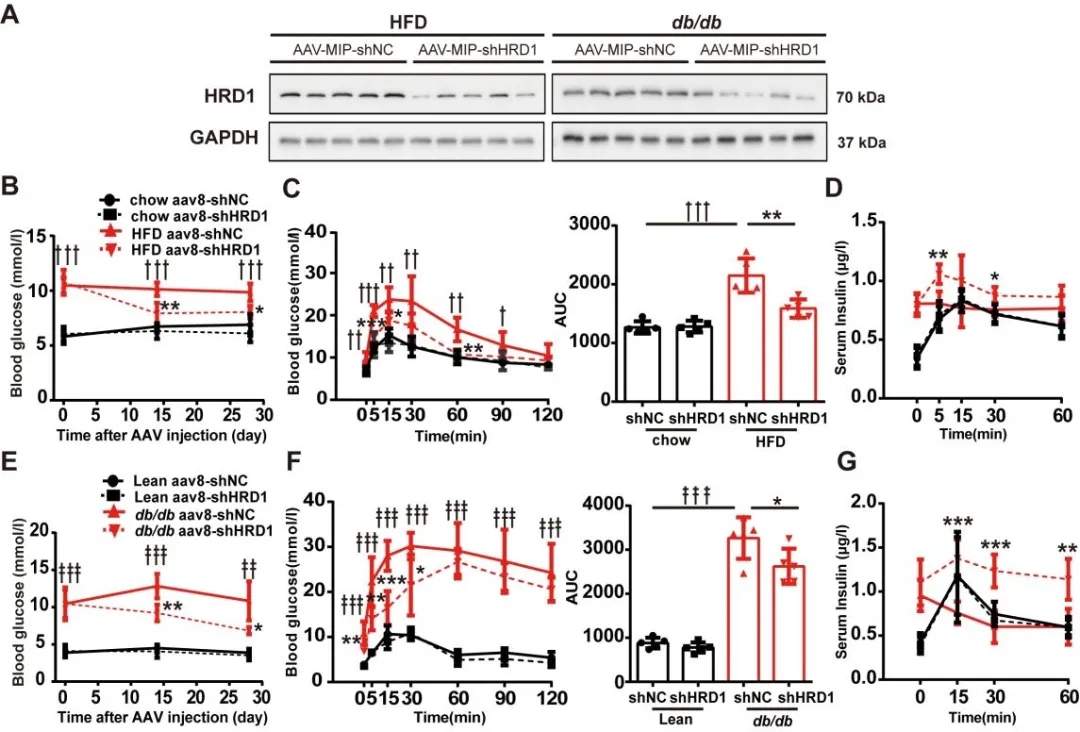
随后作者将AAV8-MIP-shHRD1(维真生物提供)注射入HFD饲喂的糖尿病小鼠胰腺导管,2周后,糖尿病小鼠空腹血糖明显下降。4周后,糖耐量试验(Intraperitoneal Glucose Tolerance Test,IPGTT)结果显示糖尿病小鼠血糖反应和血清胰岛素水平明显改善。AAV-shHRD1注射db/db小鼠的葡萄糖反应也有改善。综上结果表明HRD1在胰岛β细胞功能障碍和糖尿病中发挥重要作用。
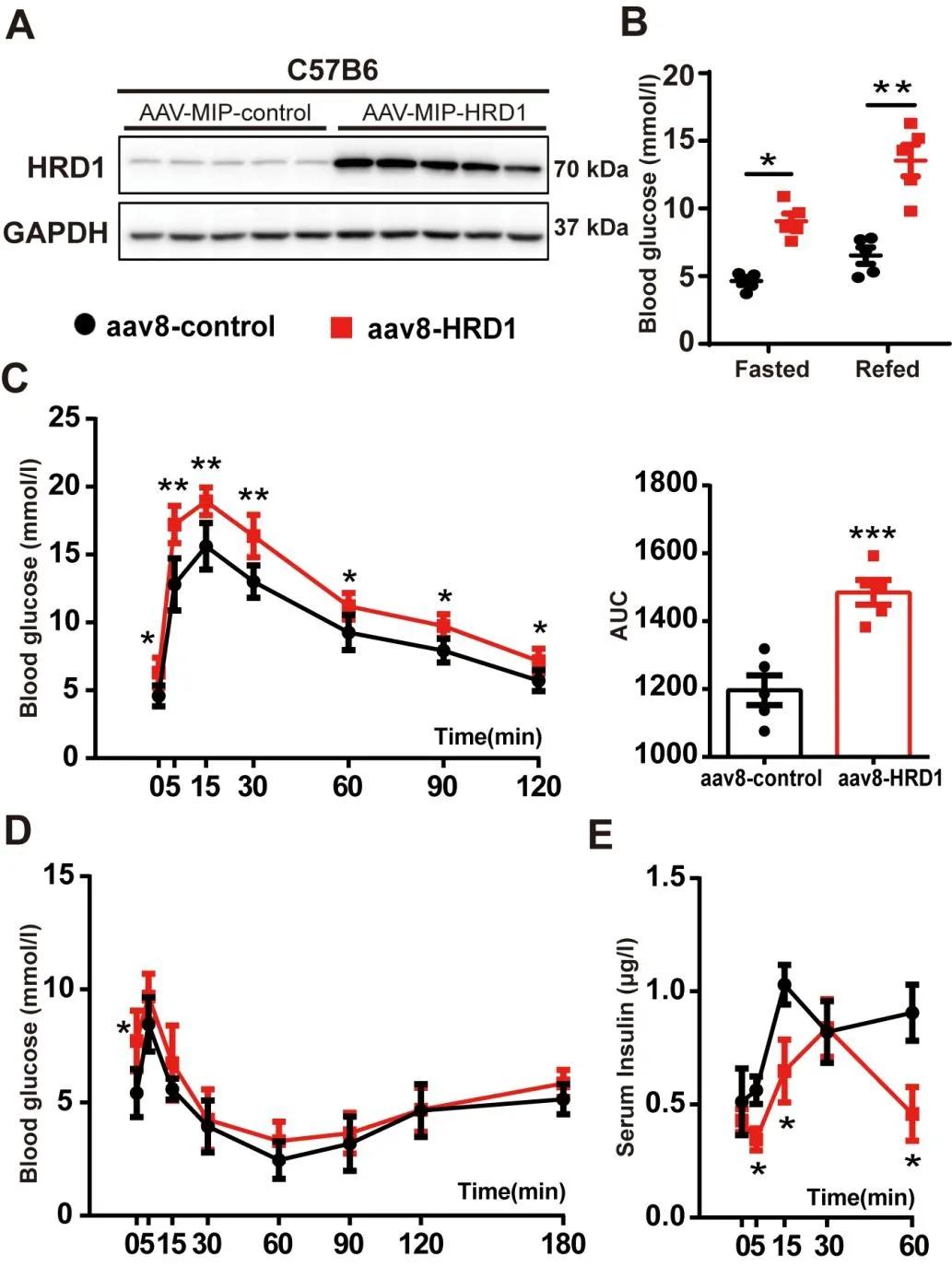
作者胰腺导管内注射AAV8-MIP-HRD1(维真生物提供),注射后胰岛HRD1蛋白水平明显升高,小鼠的空腹血糖和复餐血糖水平显著升高,获得β细胞HRD1特异性过表达小鼠。IPGTT结果显示糖代谢严重受损,HRD1特异性过表达的小鼠血浆胰岛素水平表现紊乱。上述结果表明β细胞HRD1上调可诱发高血糖并损伤胰岛素的分泌。
为了确定HRD1高表达引起的β细胞胰岛素分泌受损的分子基础,作者通过质谱分析研究Ad-HRD1 或 Ad-GFP感染后MIN6细胞HRD1的结合蛋白,发现其中一种蛋白细胞特异性转录因子MafA与碳水化合物刺激反应有关,免疫沉淀分析证实HRD1和MafA共存于沉淀复合物中,当HRD1高表达时,HRD1和MafA的相互作用增强,在人胰岛证实HRD1和MafA之间呈负相关。MafA是β细胞功能和健康的积极指标,HRD1过表达在翻译水平而非转录水平上显著降低了MafA的表达。

免疫沉淀分析证实HRD1和MafA同时存在于沉淀复合物中,HRD1和MafA之间呈负相关作用,当HRD1高表达时,二者的相互作用增强。此外,HRD1过表达在翻译水平而非转录水平上显著降低了MafA的表达。
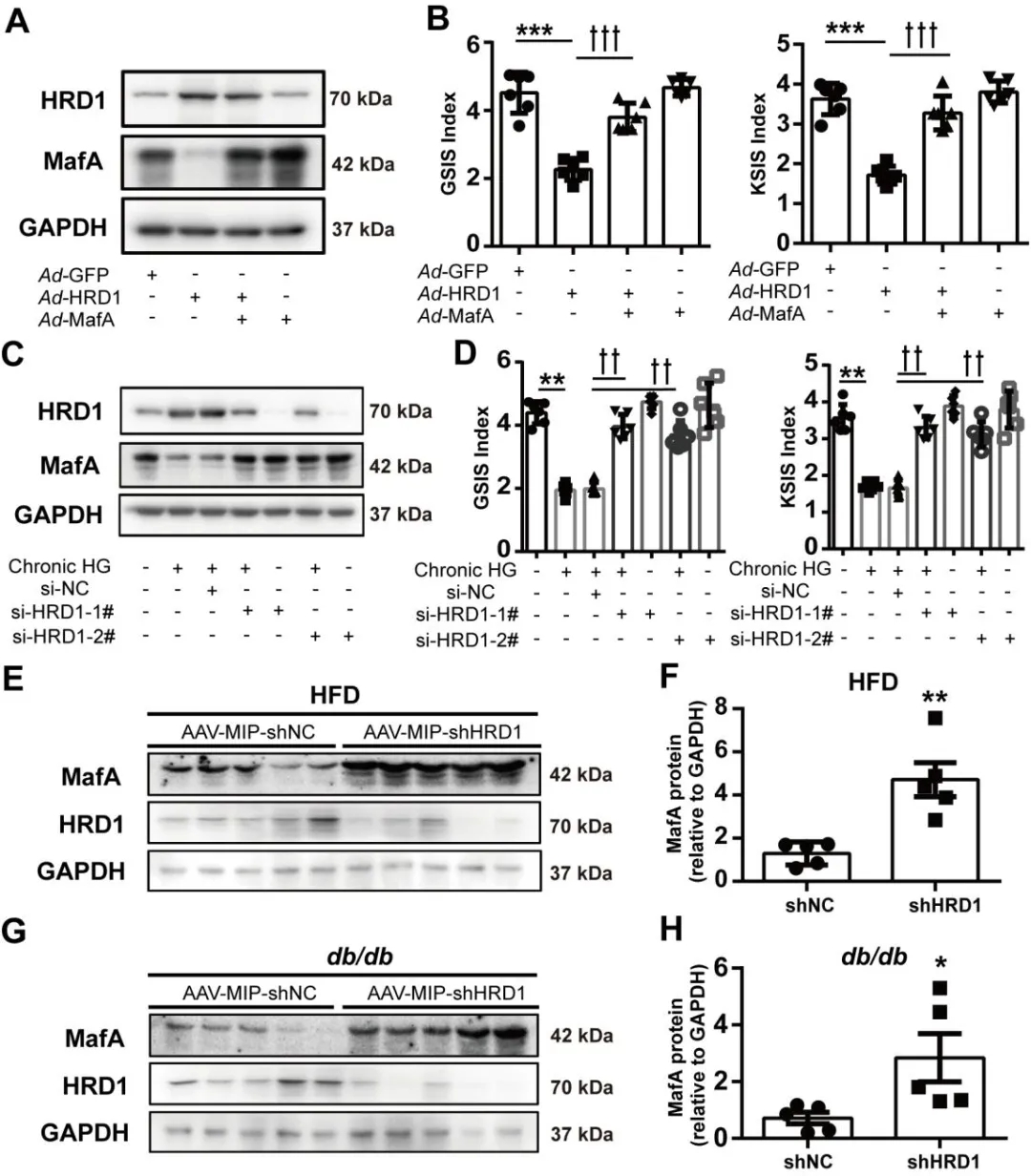
作者研究发现单独感染Ad-HRD1的小鼠胰岛和MIN6细胞,胰岛素分泌明显被抑制,这种抑制可通过补充MafA得以恢复。敲除HRD1可有效减轻因暴露于慢性高糖环境而导致的小鼠胰岛和MIN6细胞MafA的减少。小鼠胰岛细胞和长期暴露高糖环境的MIN6细胞HRD1敲除后,葡萄糖或KCL刺激的胰岛素分泌也得到了恢复。HFD饲喂的小鼠和db/db小鼠,AAV-shHRD1注射4周后,胰岛MafA表达水平也出现反弹。综上所述,HRD1高表达通过下调MafA使β细胞发生功能障碍。
在HRD1过表达时,在MIN6细胞及HEK293A细胞,MafA和HRD1定位于细胞核周围而不是细胞核,主要在ER区域共定位,表明HRD1在ER附近捕捉MafA,通过其胞质C端结构域与胞质MafA相互作用。荧光素酶报告基因检测,作者发现HRD1过表达显著降低MafA的核转录调控活性,qPCR和ChIP-qPCR结果证实胰岛素是MafA调控的主要基因。HRD1的敲低部分挽救了糖脂毒性条件下核MafA的减少,表明HRD1的降低足以维持核MafA水平。HRD1不仅调节细胞内MafA的数量,而且调节其在β细胞中的定位。

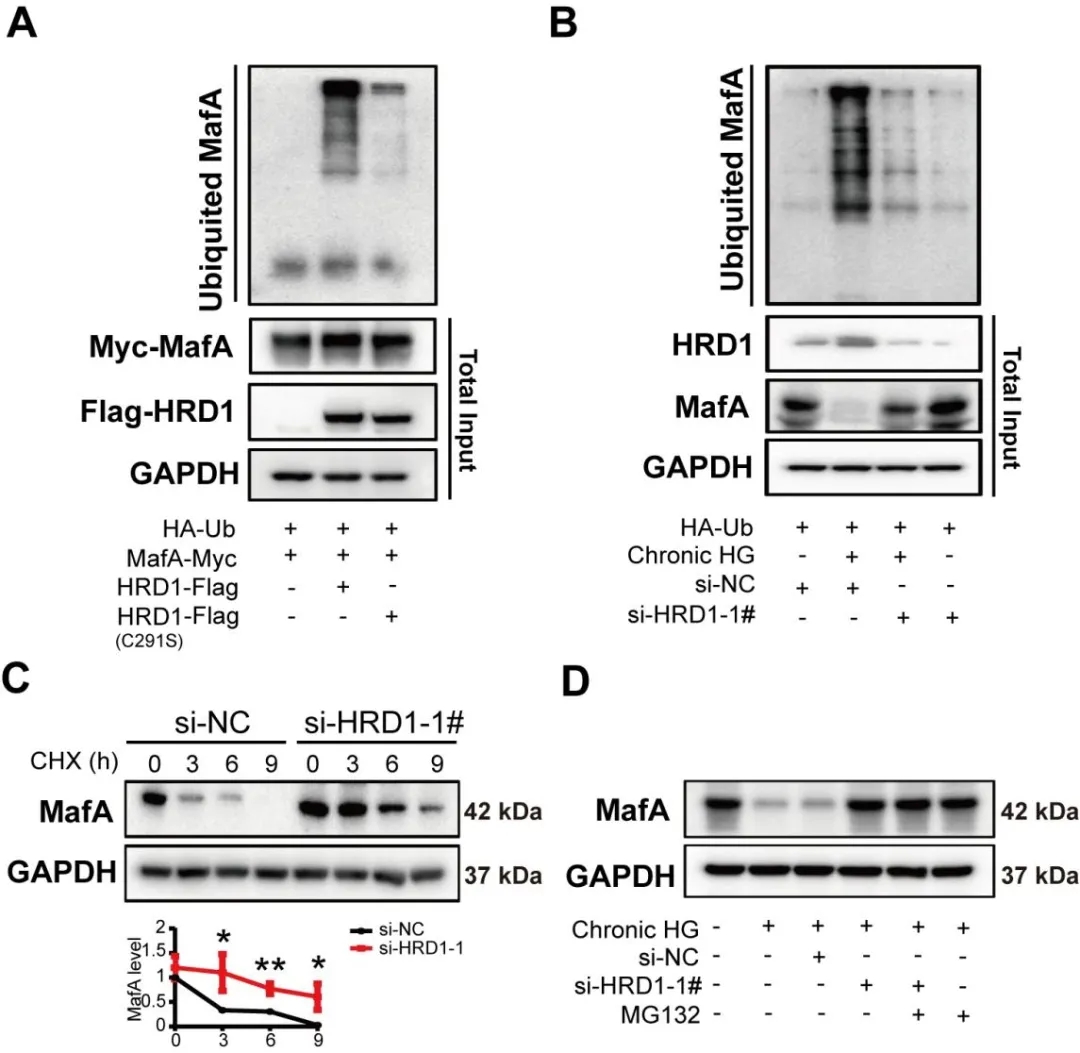
HRD1泛素连接酶的活性离不开其Ring环域内的第291位半胱氨酸,作者测量了HRD1- WT及C291S突变体HRD1 (HRD1- C291S)对MafA泛素化的影响,发现HRD1- WT过表达显著增加MafA泛素化;HRD1下调可显著降低慢性高糖处理MIN6细胞MafA的泛素化,HRD1的缺失抑制高糖环境下MafA蛋白的快速降解,并恢复MIN6细胞总MafA蛋白的下降。上述结果表明HRD1是E3泛素连接酶,其作用是负责MafA的泛素化和降解。
本研究揭示HRD1作为E3泛素连接酶介导MafA的泛素化和降解,它的失调(缺失或过量)可导致胰岛β细胞功能衰竭,在糖尿病的发病机理中起着重要的作用。针对HRD1靶向治疗可提高MafA的蛋白水平,改善β细胞功能,治疗2型糖尿病。
产品:
AAV8-MIP -shHRD1-GFP
AAV8-MIP-HRD1-GFP
AAV8-control
滴度:1012 GCP/ml
注射方式:胰腺导管内注射
1. Hu Y, Gao Y, Zhang M, Deng KY, Singh R, Tian Q, Gong Y, Pan Z, Liu Q, Boisclair YR,Long Q. 2019. Endoplasmic Reticulum-Associated Degradation (ERAD) Has a Critical Role in Supporting Glucose-Stimulated Insulin Secretion in Pancreatic beta-Cells. Diabetes 68: 733-46 .
2. Meier, J.J., [Treatment of type 2 diabetes]. Internist (Berl), 2016. 57(2): p. 153-65.