当前位置:首页 > 研究领域 > 消化系统
当前位置:首页 > 研究领域 > 消化系统
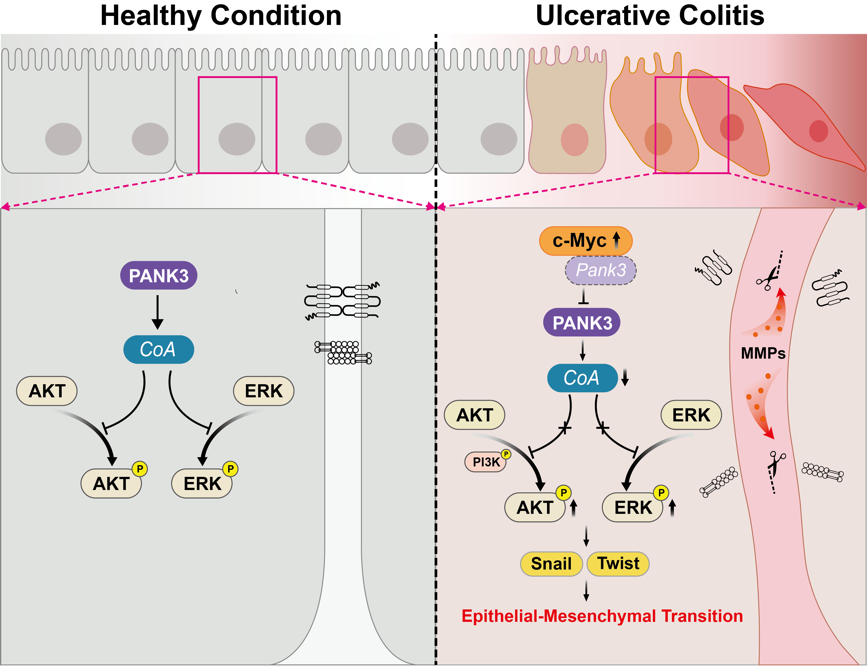
炎症性肠病(IBD)含溃疡性结肠炎(UC)和克罗恩病(CD),呈慢性复发性,全球患病率激增,现有治疗存在疗效不佳、复发率高、副作用明显等问题。肠道屏障是肠道稳态的核心,其损伤先于IBD疾病进展,修复屏障完整性是IBD治疗的重要方向,但相关机制未明确,缺乏有效靶点。2025年12月,中国药科大学阿基业/王广基/谢媛联合江苏省中医院肖君团队在Journal of Advanced Research (IF13.0)期刊发表题为”c-Myc-PANK3-EMT axis regulates the structure and function of intestinal barrier in ulcerative colitis c-Myc-PANK3-EMT axis regulates UC intestinal barrier integrity“的研究论文。文章揭示了c-Myc-PANK3-EMT 轴在维持肠屏障结构和功能完整性中发挥关键作用,PANK3是UC肠屏障修复的潜在靶点,而叶酸是PANK3的候选激动剂。

| 基因信息 | 泛酸激酶3(PANK3) |
|---|---|
| 实验动物 | 6周龄雄性C57BL/6J小鼠 |
| 病毒产品 |
AAV9-CMV-PANK3-P2A-GFP (4.64×1013 vg/mL)、AAV9-CMV-GFP (6.50×1013 vg/mL); AAV9-CMV-4in1shRNA-PANK3-GFP(2.27×1013vg/mL)、AAV9-CMV-Scramble-GFP (5.53×1013 vg/mL) |
| 注射方式 | 灌肠 |
| 病毒用量 | 100 µL,1.0×1011 vg/mouse |
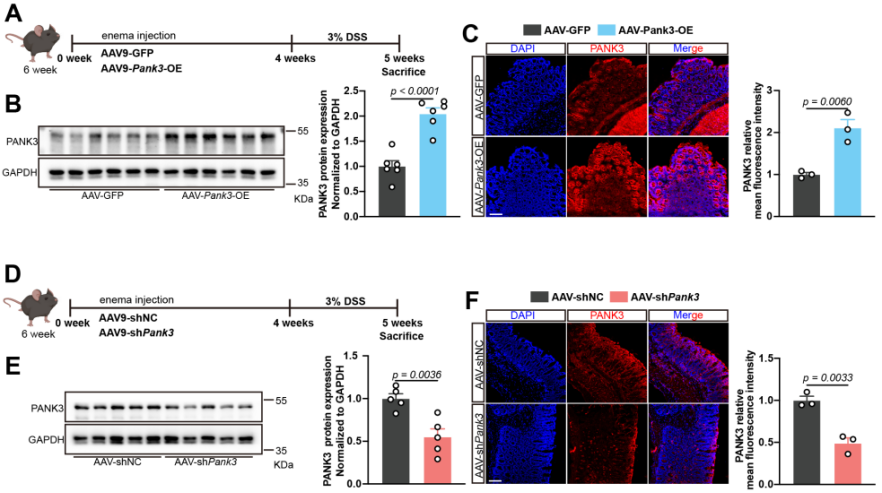
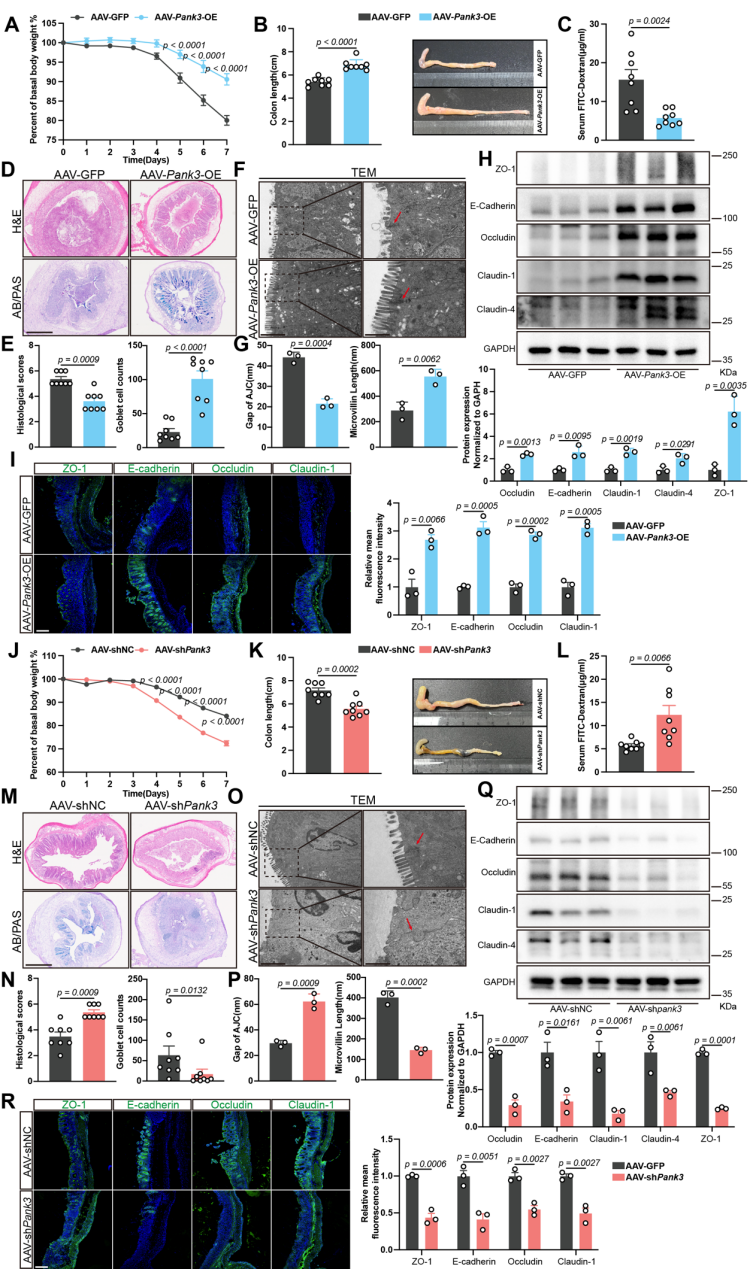
研究团队通过代谢组学分析发现UC小鼠结肠中泛酸水平升高,提示泛酸代谢异常,此外在UC患者、DSS诱导的小鼠结肠炎模型和IL-10敲除模型中,PANK3的mRNA和蛋白表达均显著下降。进一步使用TNF-α和IFN-γ处理人结肠上皮细胞HT29和NCM460模拟炎症环境,结果显示PANK3激动剂或过表达可增强细胞间连接蛋白表达,对肠上皮屏障的完整性具有保护作用,抑制PANK3则起相反作用。随后使用PANK3激动剂治疗DSS诱导的结肠炎小鼠,PZ-2891治疗显著逆转体重减轻和结肠缩短,并改善组织学特征和肠道通透性,相反PANK3抑制剂则加重结肠炎损伤。考虑到药理学调节的脱靶效应的可能性,研究人员利用AAV9过表达或敲低PANK3,特异性调控肠道PANK3基因表达,进一步证实PANK3过表达可减轻结肠炎症状、改善肠屏障结构和功能;敲低PANK3则加重病情。上述结果表明PANK3在改善UC引起的肠屏障损伤中起关键作用。
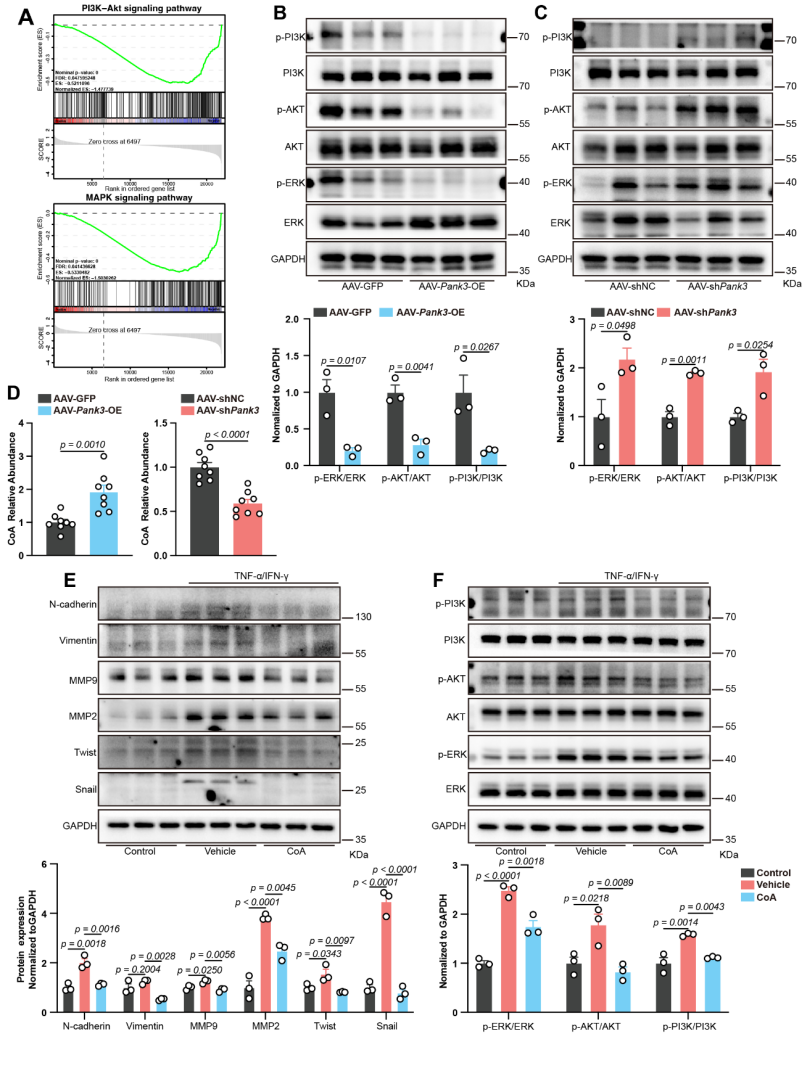
转录组分析揭示PANK3抑制EMT相关基因,差异表达基因显著富集于细胞迁移、黏附、运动及ECM重塑等生物学过程,这些均为EMT的特征性事件;并且PANK3过表达抑制EMT标志物表达,PANK3敲低则促进EMT表型,表明PANK3通过转录调控抑制EMT相关基因的表达,从而在炎症环境中维持上皮表型、阻止间质转化,进而保护肠屏障的结构与功能完整性。基因集富集分析显示,在AAV-Pank3-OE小鼠中,PI3K/AKT和MAPK信号通路的基因集显著被抑制,这些通路是已知的EMT上游调控通路;此外,PANK3过表达显著降低PI3K、AKT和ERK的磷酸化水平,PANK3敲低则导致这些信号分子磷酸化水平升高。体外实验表明,完全去除泛酸(PANK3底物)会取消PANK3激动剂或过表达对屏障的保护作用,说明PANK3的功能依赖于其代谢酶活性。LC-MS/MS定量分析显示PANK3过表达显著提高结肠组织中游离CoA水平,敲低则降低CoA水平,HT29细胞中外源性补充CoA可抑制EMT及下游信号通路。这些数据表明,上调PANK3通过增强CoA合成来抑制MAPK和PI3K/AKT信号级联反应,并抑制活化的上皮-间质转化。
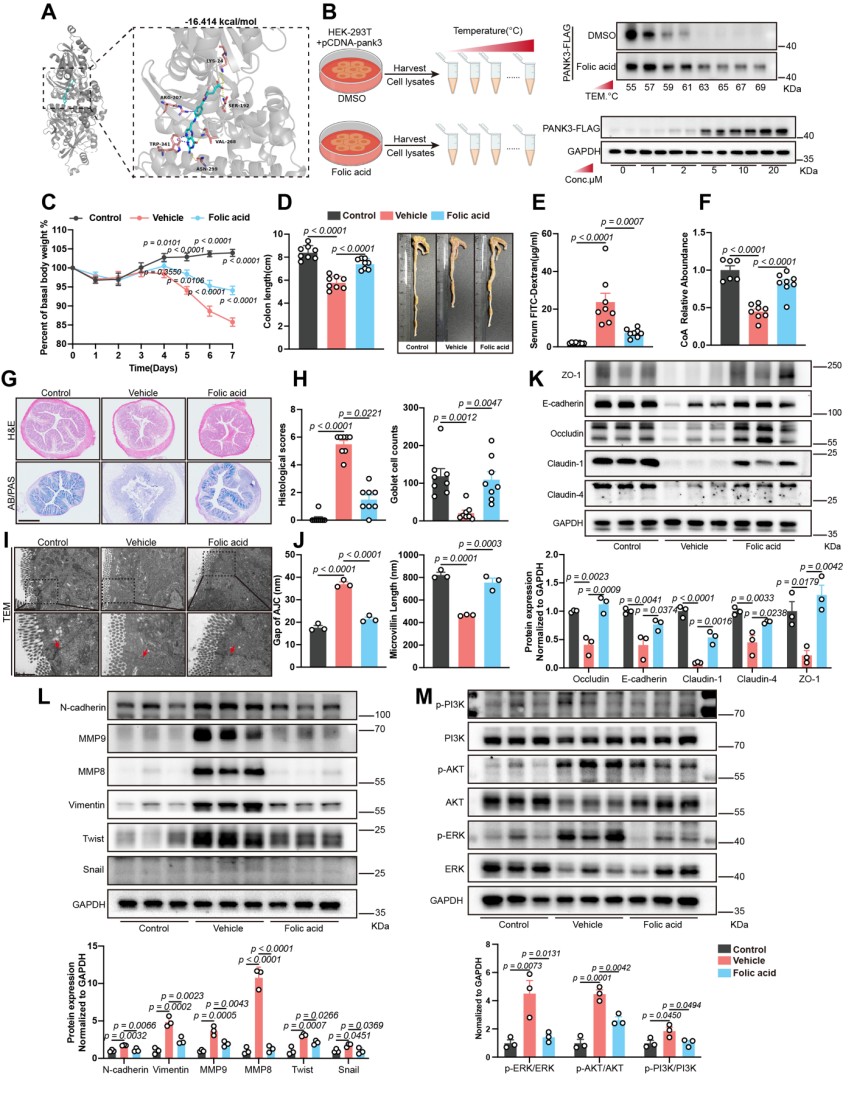
进一步的探索证实c-Myc是调控PANK3表达和功能的关键转录因子,c-Myc-PANK3轴在肠屏障破坏中起关键作用。通过高通量虚拟筛选结合分子对接分析,发现叶酸与PANK3的关键结合残基(Lys24, Ser192, Arg207等)具有稳定相互作用。细胞热位移实验证实叶酸能够剂量依赖性地增强PANK3蛋白的热稳定性,直接证明其结合作用。接下来研究团队在DSS诱导的UC模型中评估了叶酸的治疗潜力,口服30 mg/kg叶酸后,UC的病理特征明显改善,包括进行性体重减轻、结肠长度缩短和肠屏障破坏;重要的是,叶酸显著刺激PANK3的功能,提高结肠CoA水平并恢复上皮结构,并调控屏障与EMT相关蛋白表达。然而叶酸对肠屏障的保护作用在PANK3敲低后被取消,证明其作用具有PANK3依赖性。综上,这些发现表明叶酸作为PANK3的潜在激动剂发挥作用,可以改善肠道屏障完整性并改善DSS诱导的结肠炎。
本研究确立了c-Myc-PANK3轴在溃疡性结肠炎肠道上皮屏障损伤中的核心作用。具体而言,炎症触发c-Myc介导的PANK3转录抑制,导致CoA合成受阻,并通过PI3K/AKT和MAPK信号通路启动上皮-间质转化过程。恢复PANK3的表达与功能可有效改善肠道屏障功能障碍和实验性结肠炎。这些发现凸显了PANK3作为溃疡性结肠炎新型治疗靶点的潜力,并支持其已鉴定的激动剂叶酸的临床转化前景。