IF 9.685|田德安/项涛教授研究团队揭示非酒精性脂肪性肝病和慢性肾脏疾病间的关联机制
越来越多的流行病学证据表明,非酒精性脂肪性肝病(NAFLD)是慢性肾脏疾病(CKD)的独立危险因素,但NAFLD与CKD之间的调节机制尚不清楚。2023年,华中科技大学同济医学院附属同济医院田德安/项涛教授在Cell Death & Disease (IF 9.685)上发表题为“Genetic deletion of phosphodiesterase 4D in the liver improves kidney damage in high-fat fed mice: liver-kidney crosstalk”的研究论文。该研究指出脂肪肝高表达的PDE4D通过TGF-β1-SMAD信号介导肾损伤,揭示PDE4D可能是NAFLD和相关肾损伤之间的关键介质,同时证明PDE4抑制剂罗氟司特是NAFLD相关CKD的潜在治疗策略。


研究结果分享
1、肝脏PDE4D缺乏改善了HFD诱导的肝脂肪变性和相关肾损伤
高脂肪饮食(HFD)是NAFLD和肾功能障碍的致病因素,作者发现HFD喂养后小鼠肝脏PDE4D表达显著增加,而肾脏PDE4D表达不变。随后构建了肝脏特异性PDE4D敲除(PDE4D-LKO)小鼠,高脂喂养后,PDE4D-LKO小鼠的异常代谢不仅得到明显好转,HFD诱导的肝脏肿胀和脂质沉积也大大减轻。进一步分析发现,PDE4D-LKO小鼠肾脏对胰岛素敏感性增加,此外小鼠的肾脏重量和肾周脂肪重量显著降低,肾功能也得到改善。这些发现表明肝脏PDE4D缺乏改善了HFD诱导的肝脂肪变性和相关的肾损害。
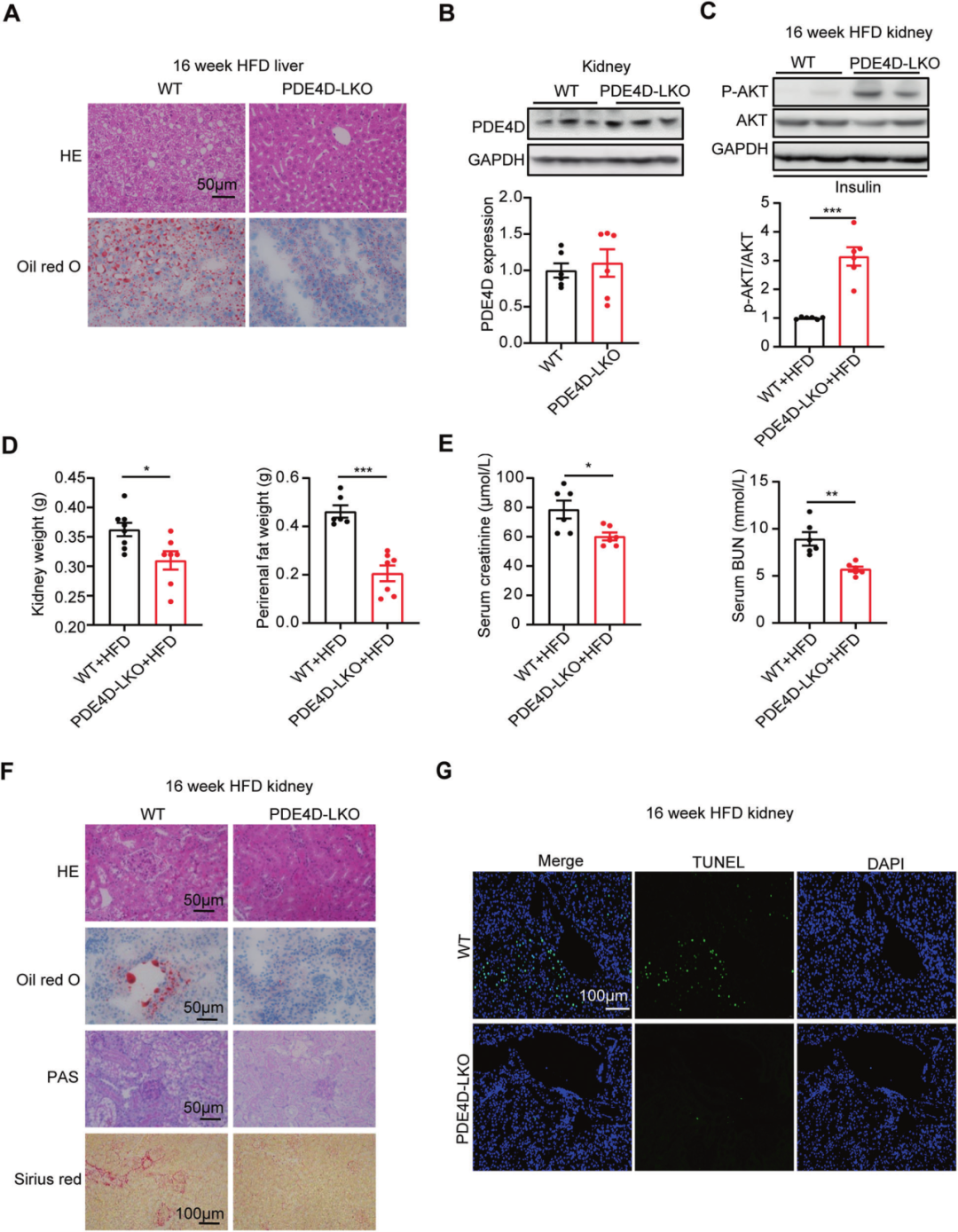
图1. 肝脏PDE4D缺乏改善了HFD诱导的肝脂肪变性和相关的肾损害
2、AAV介导的PDE4D过表达加重肾损伤
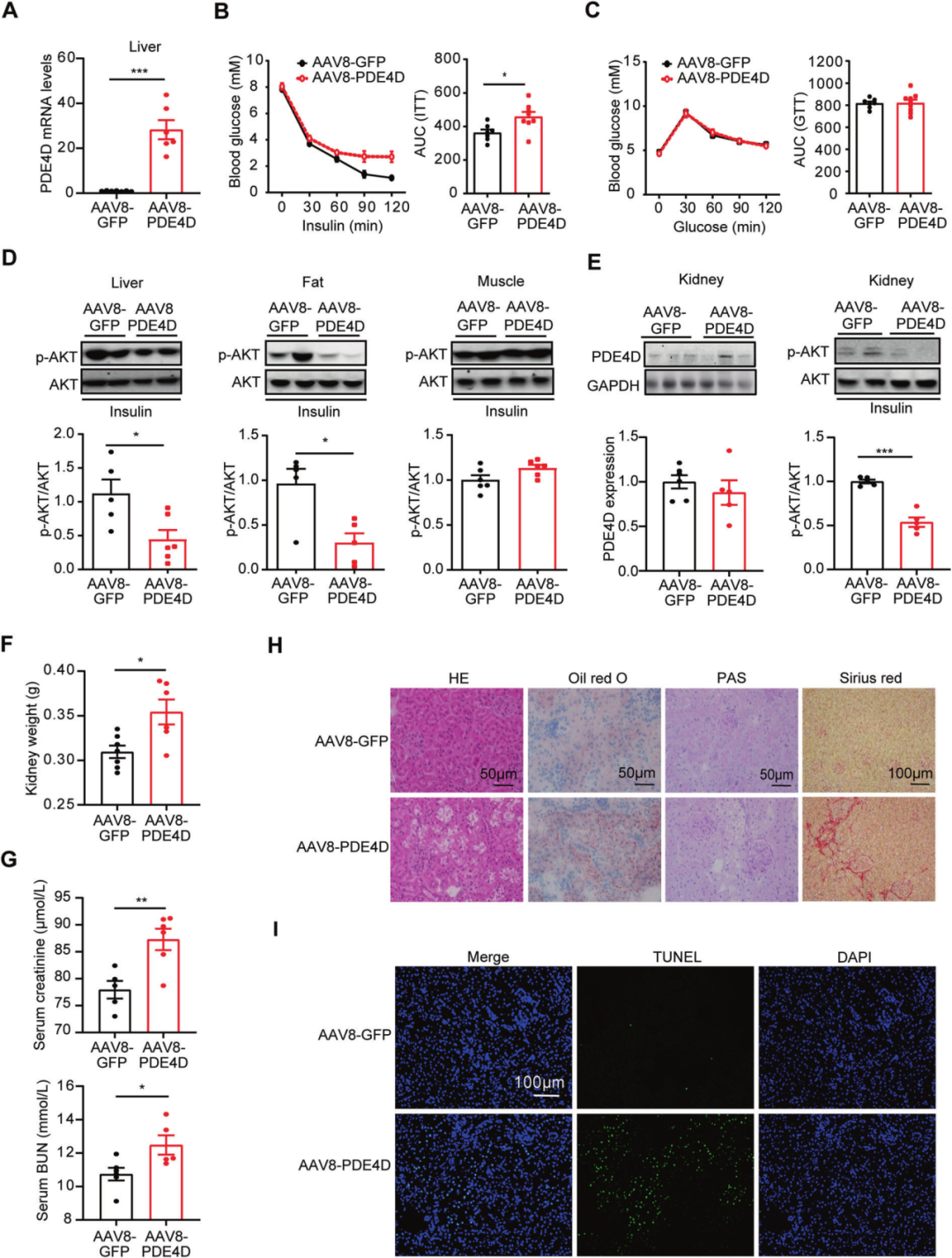
作者先前的研究表明PDE4D在肝脏中过表达可诱导肝脂肪变性。为了进一步研究肝脏PDE4D对肾脏结构和功能的影响,研究人员借助AAV8病毒载体实现了小鼠肝脏中PDE4D的过表达。分析发现AAV8-PDE4D处理的小鼠表现出胰岛素耐受以及肝脏胰岛素信号的受损;不仅如此,小鼠肾脏胰岛素信号也受到损害。此外,肝脏中PDE4D的过表达导致肾脏发生损伤,并伴有肾脏重量增加、血清肌酐和BUN水平升高,以及胶原积累和细胞凋亡增加。这些结果表明肝脏PDE4D的过表达在NAFLD和肾损伤中起关键作用。
图2. AAV介导的PDE4D过表达加重肾损伤
3、肝脏PDE4D通过TGF-β1途径介导NAFLD相关肾损伤
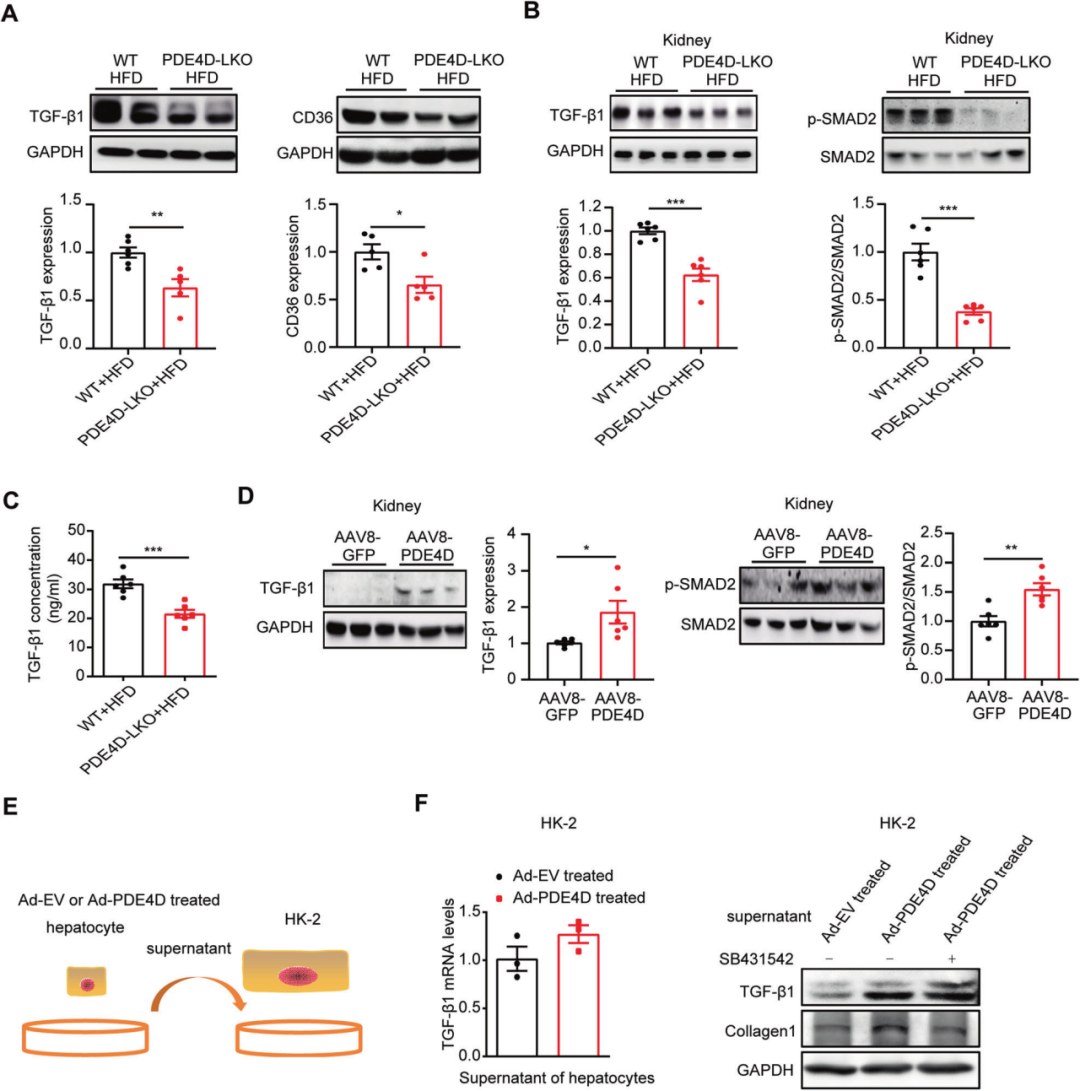
大量研究表明,TGF-β是CKD中驱动纤维化的主要因素,其通过激活Smad依赖性和Smad非依赖性信号通路起作用。作者前期的研究表明PDE4D过表达足以通过CD36-TGF-β1通路触发NAFLD,在此研究人员发现肝脏PDE4D基因缺失确实导致TGF-β1和CD36蛋白水平下降,并显著降低HFD喂养小鼠肾脏中TGF-β1的表达、SMAD2的磷酸化以及血清中循环TGF-β1的水平;相反,AAV8-PDE4D处理小鼠肾脏中TGF-β1和p-SMAD2蛋白水平显著升高。体外用感染Ad-PDE4D或Ad-EV的肝细胞上清液处理HK-2细胞,同样得到了类似的结果。表明,TGF-β1可能在肝脏PDE4D介导的NAFLD和相关CKD中发挥重要作用。
图3. 肝脏PDE4D通过TGF-β1途径介导NAFLD相关肾损伤
4、PDE4抑制剂罗氟司特可减轻高脂饮食引起的肾损伤
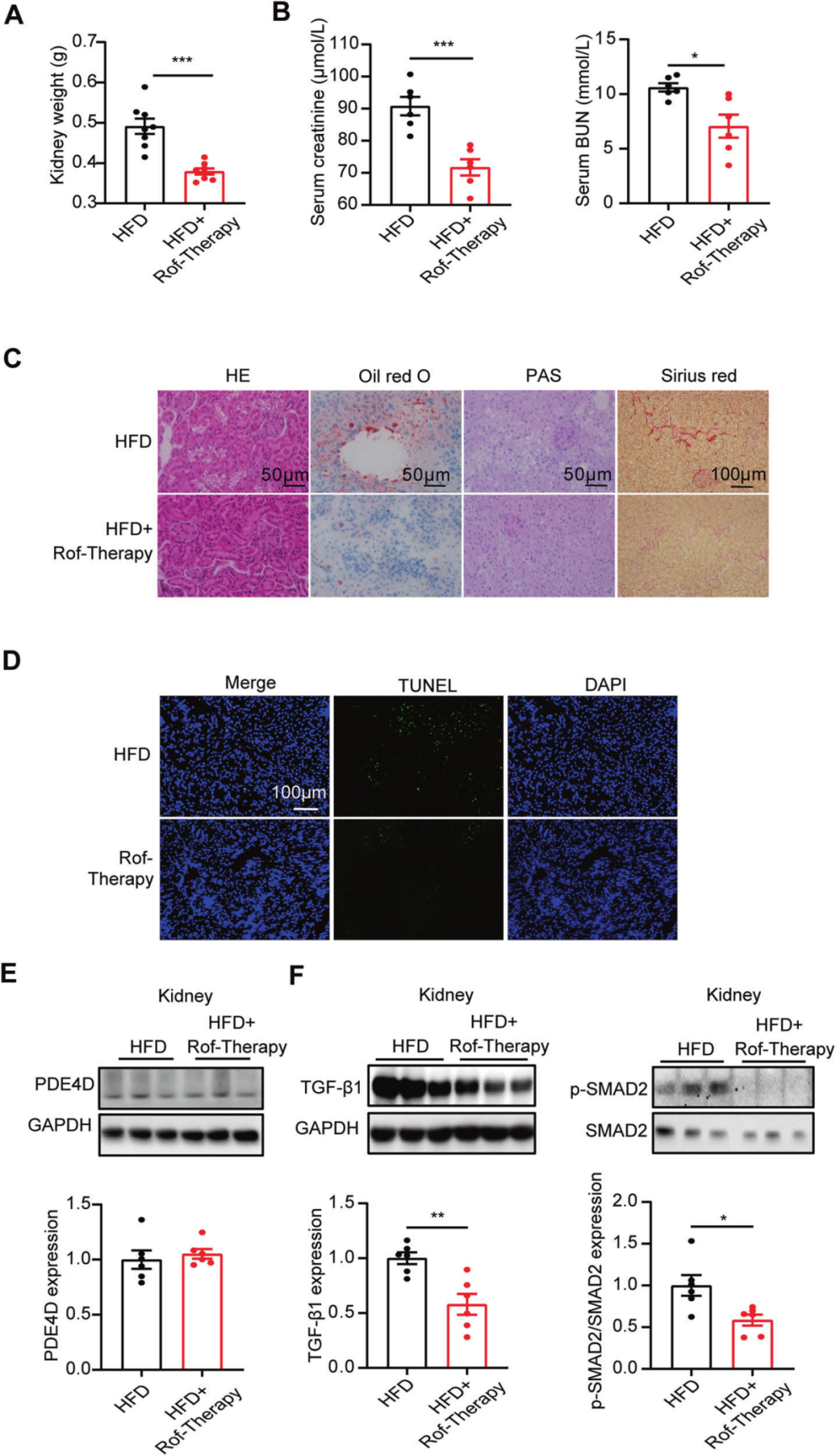
罗氟司特是一种选择性PDE4抑制剂,前期的研究证实了罗氟司特对HFD诱导的NAFLD具有治疗作用。作者研究了罗氟司特是否可以改善高脂肪饮食引起的肾损伤。HFD喂养16周后给予罗氟司特给药,4周后检测发现小鼠的肾脏重量、循环肌酐及BUN水平显著降低,同时肾脏脂质沉积减少,胶原沉积和细胞凋亡得到显著改善,此外,罗氟司特治疗降低了HFD喂养小鼠肾脏中TGF-β1和SMAD2磷酸化的蛋白表达。这些结果表明PDE4抑制剂罗氟司特可能是一种通过抑制肝脏PDE4D来预防或治疗NAFLD相关CKD的潜在方法。
图4. PDE4抑制剂罗氟司特可减轻高脂饮食引起的肾损伤
结论
本研究证明HFD喂养特异性地诱导肝脏中PDE4D的表达,PDE4D高表达加重肝脏脂质沉积和胰岛素抵抗,进而促进TGF-β1分泌入血,导致肾脏损害。肝脏PDE4D基因缺失或使用PDE4抑制剂罗氟司特治疗可有效逆转HFD诱导的肾功能障碍。这些研究结果为CKD提供了一种新的治疗策略。
 当前位置:首页 > 新闻中心 > 新闻资讯
当前位置:首页 > 新闻中心 > 新闻资讯